У сучасних промислових галузях — фармацевтиці, медицині, біотехнологіях, мікроелектроніці — критично важливо контролювати якість повітря та рівень забруднення у виробничих зонах. Саме тому все більше підприємств впроваджують чисті приміщення, створені за міжнародними вимогами. У цій статті розглянемо, що таке чисте приміщення, як визначаються класи чистоти, та які стандарти — GMP і ISO — регулюють вимоги до їхнього проєктування та експлуатації.
Що таке чисте приміщення
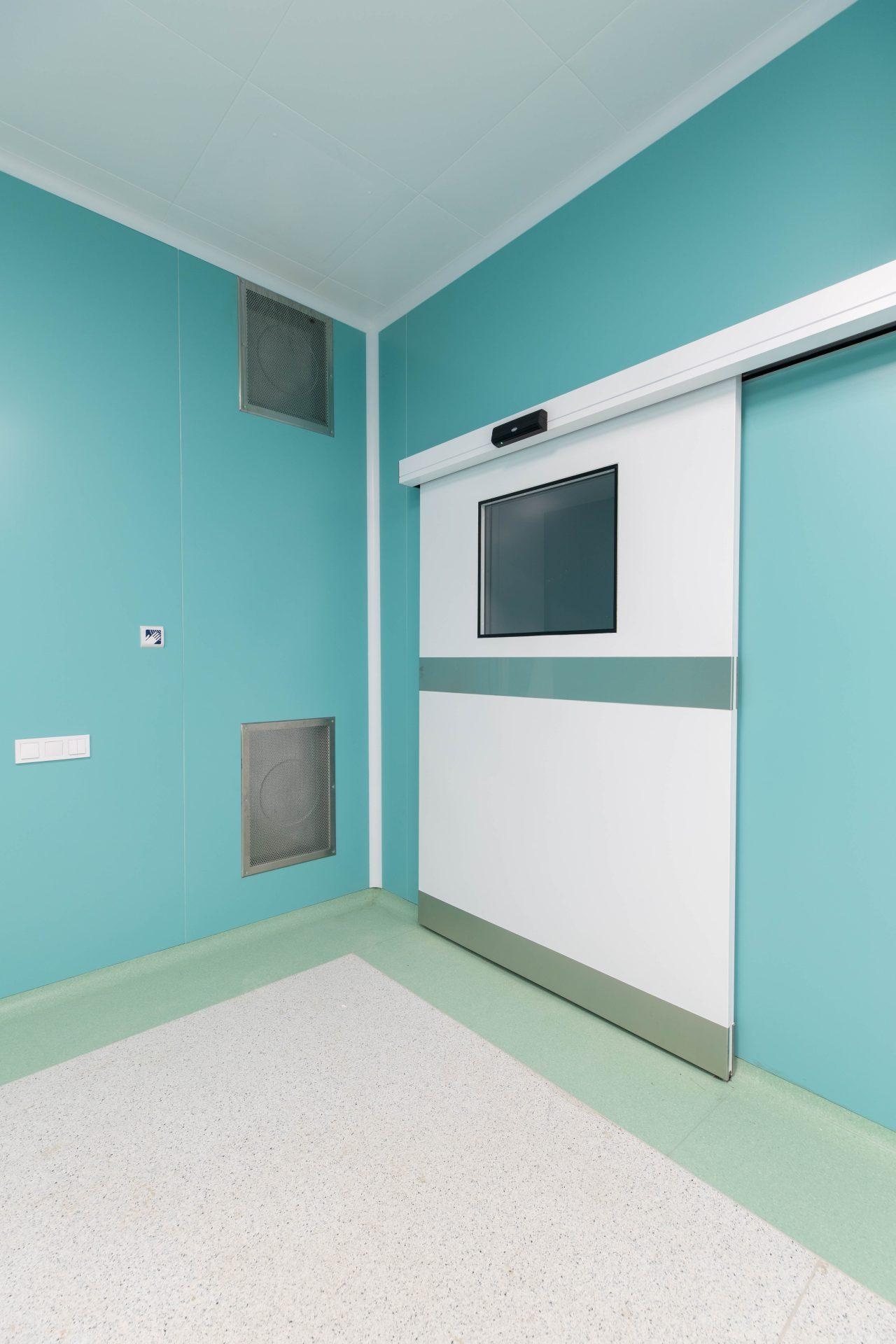
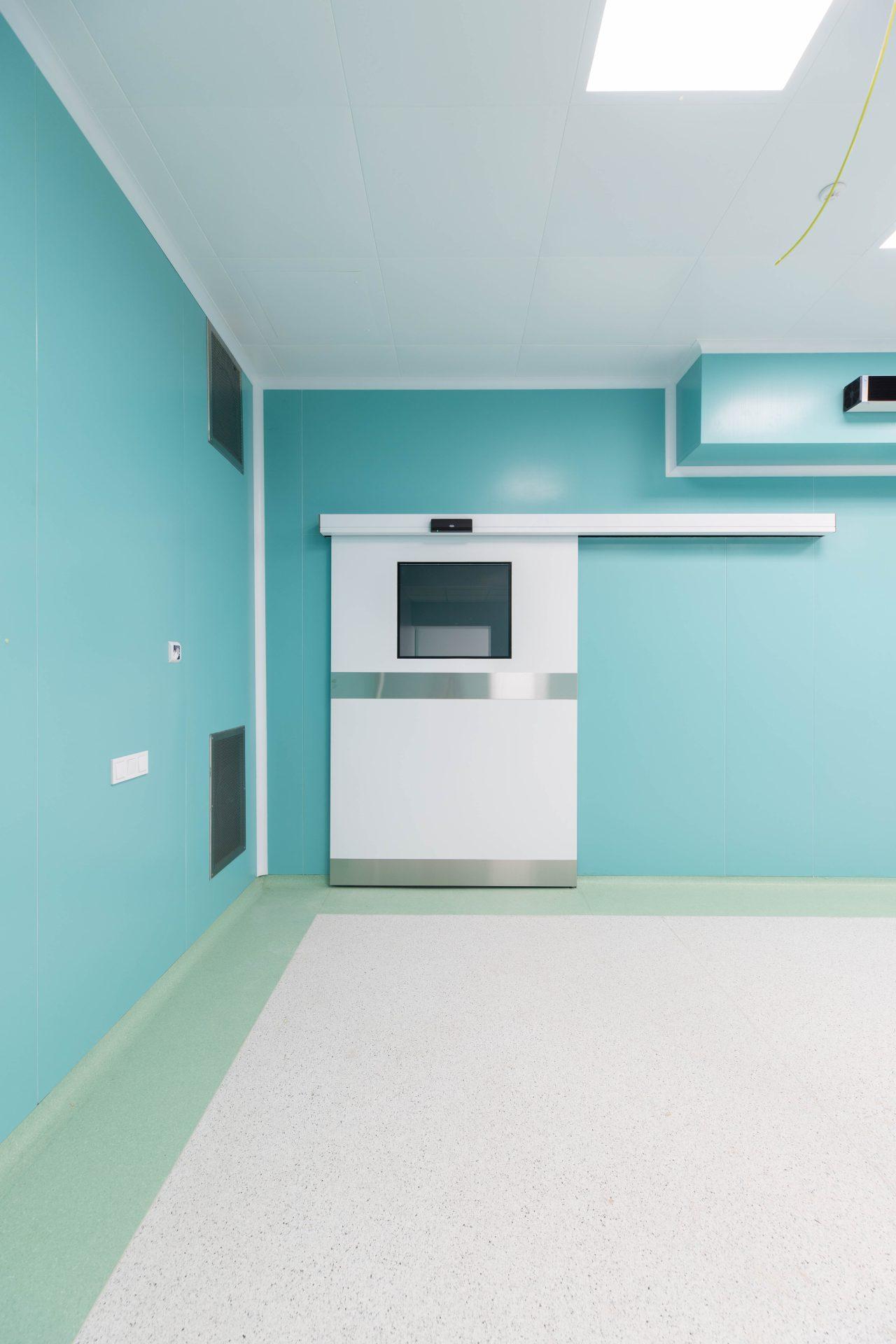
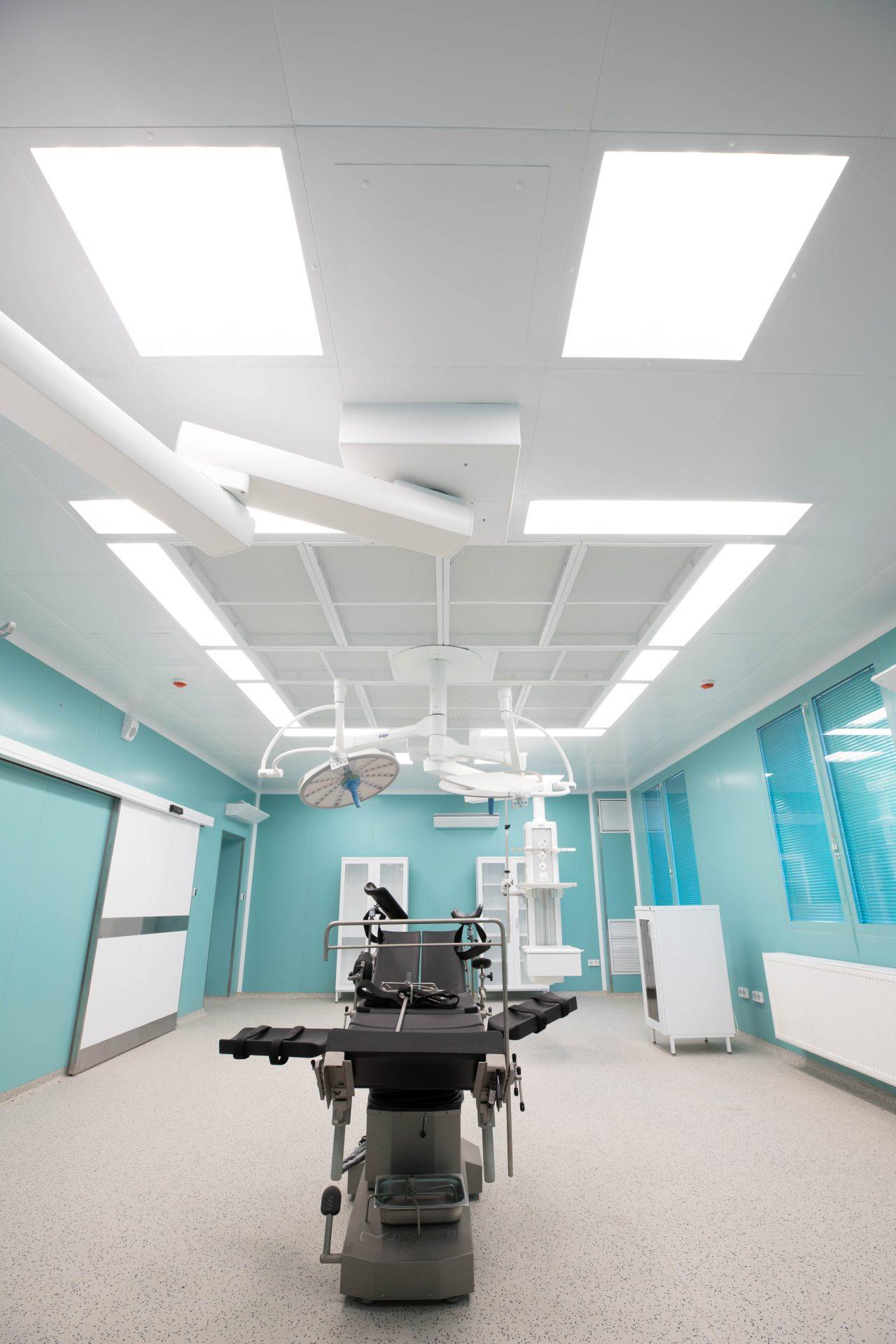
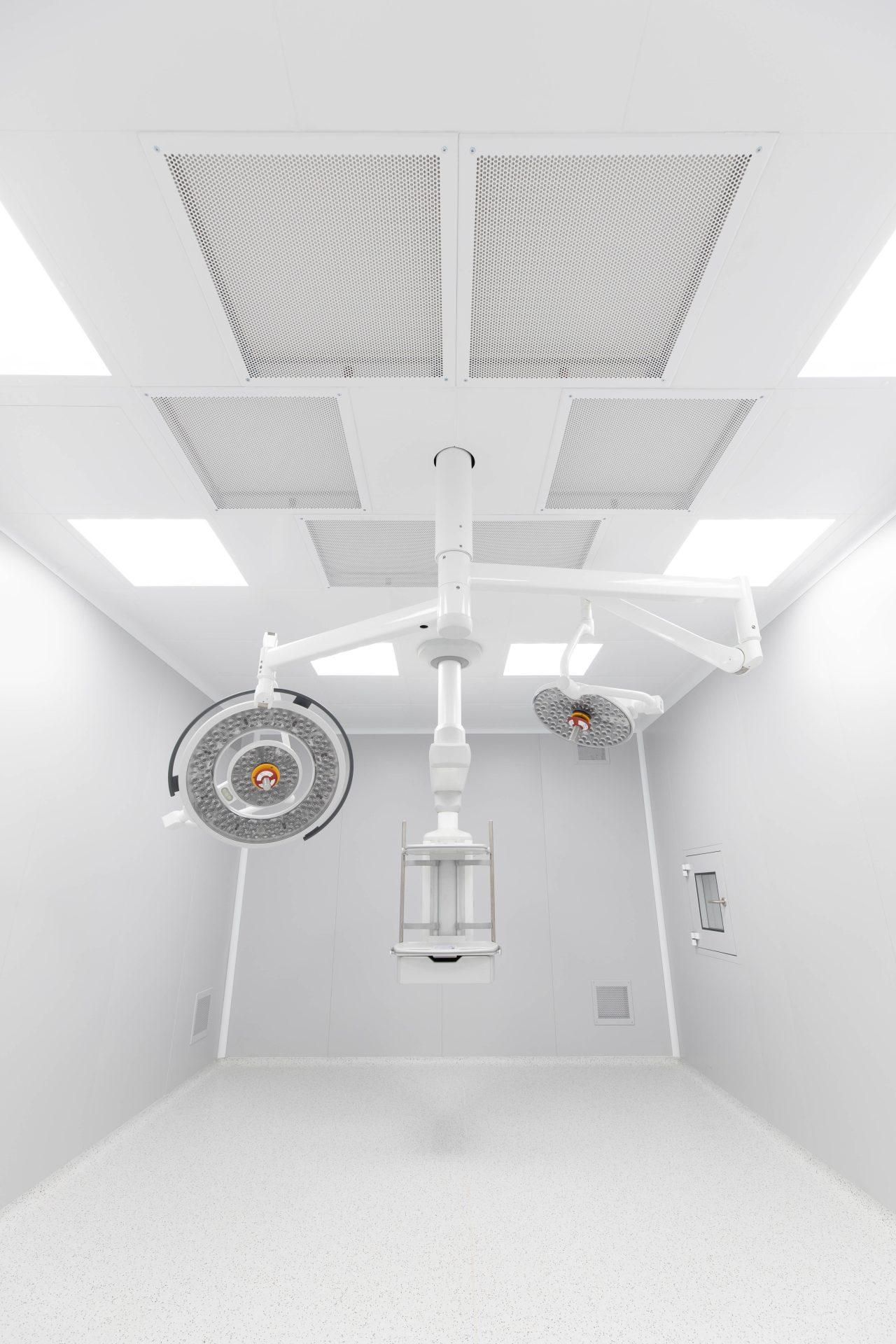
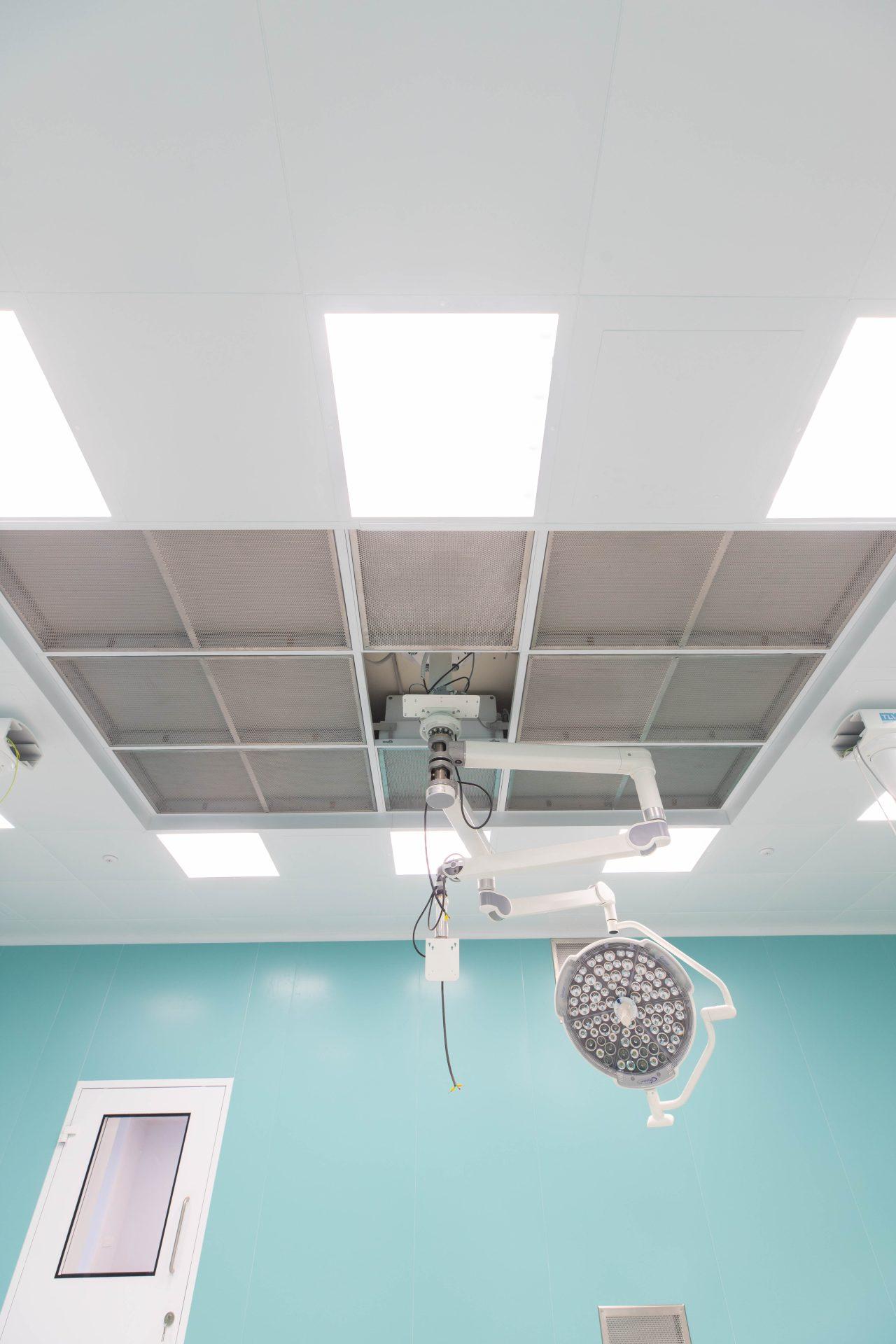
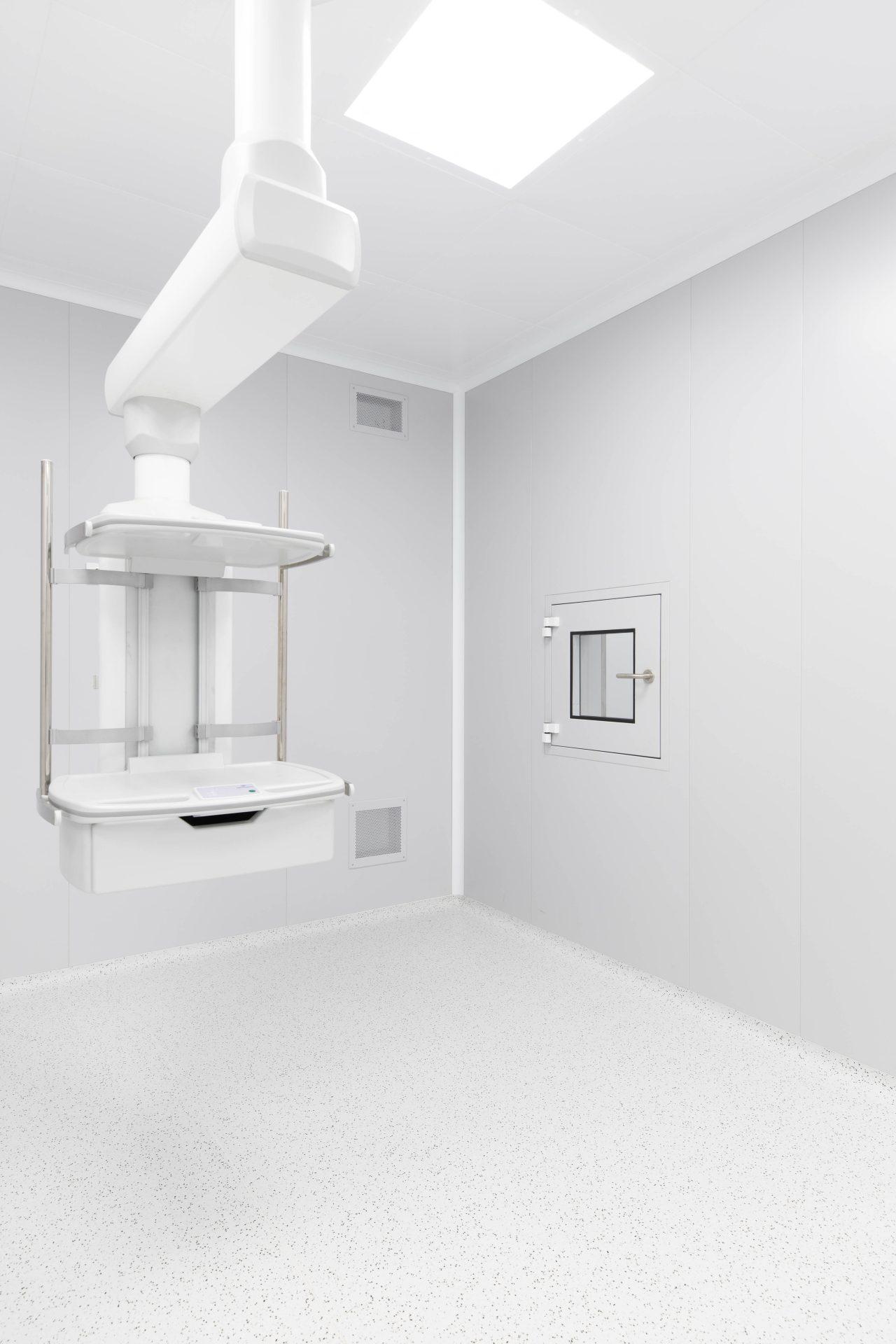
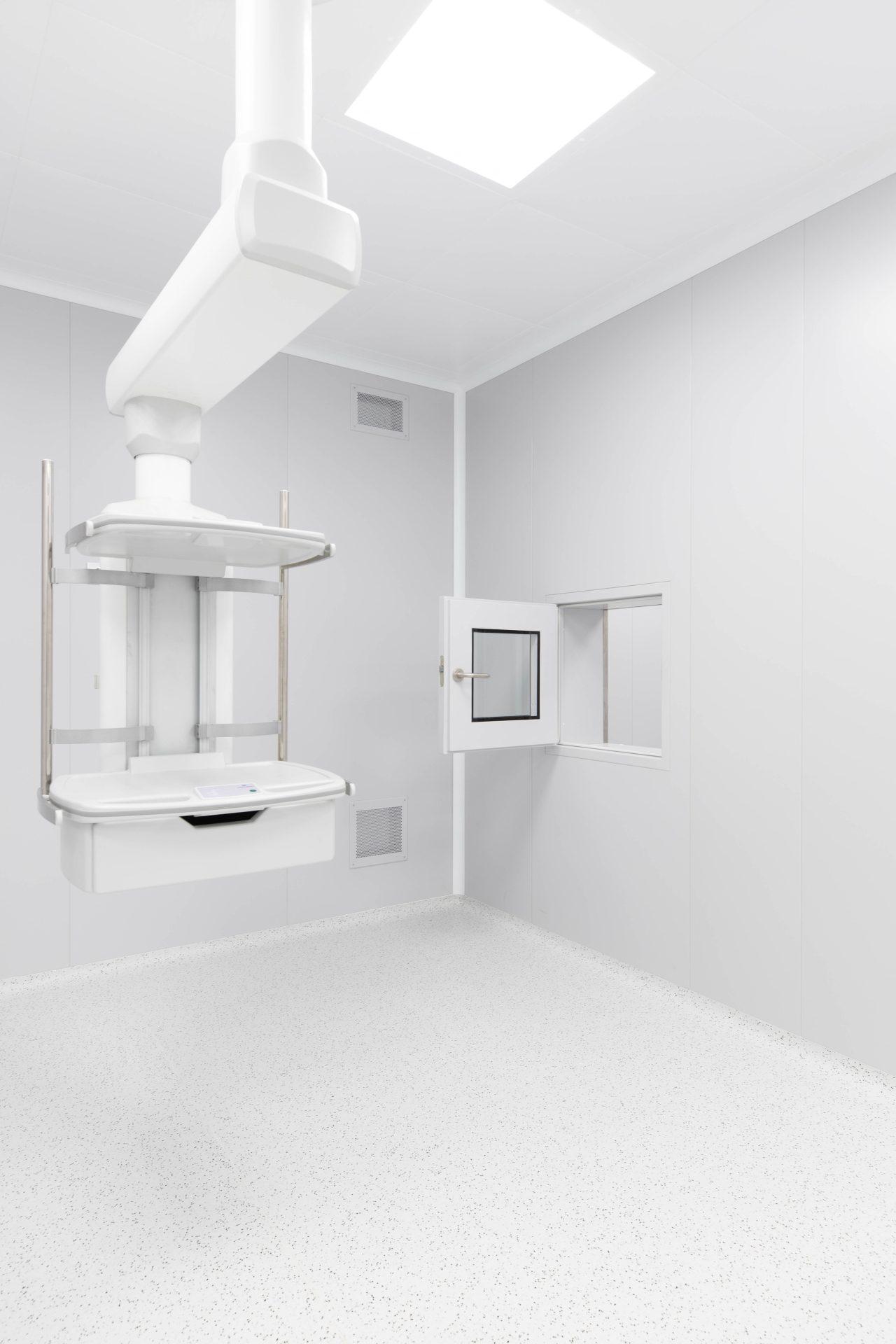
Чисте приміщення — це спеціально спроєктована зона, у якій створено контрольоване середовище з мінімальним рівнем частинок і мікроорганізмів у повітрі. Такі приміщення дозволяють проводити чутливі технологічні процеси без ризику забруднення продукції чи матеріалів.
Ключові параметри чистого приміщення:
-
рівень чистоти повітря (концентрація частинок різних розмірів);
-
контроль температури й вологості;
-
контроль перепаду тиску між зонами;
-
швидкість і напрям руху повітря;
-
антимікробні та антистатичні матеріали оздоблення;
-
контроль доступу персоналу.
Система вентиляції, конструкція приміщення та спеціальні фільтри (зокрема HEPA-фільтри) забезпечують необхідний клас чистоти, що визначається міжнародними нормами.
Чисті приміщення від Polikor
Компанія Polikor вже понад 30 років спеціалізується на виробництві та реалізації комплексних рішень для чистих приміщень, включно зі стіновими та стельовими панелями, дверними блоками та системами перегородок.
Підприємство забезпечує повний цикл — від проєктування до монтажу та сервісного супроводу. Завдяки досвіду роботи у фармацевтиці, медицині, біотехнологіях і мікроелектроніці Polikor створює системи, що стабільно відповідають вимогам GMP, ISO 14644 та українських нормативів, а також проходять міжнародні аудити. Такий підхід гарантує підприємствам надійну відповідність стандартам та ефективність виробничих процесів.
Класи чистоти: як визначається рівень контролю
Класи чистих приміщень регламентуються двома основними стандартами:
-
ISO 14644-1 — визначає рівень забруднення повітря частинками; класи ISO 1–9.
-
GMP (Good Manufacturing Practice) — регулює чистоту у фармацевтичному виробництві; класи A, B, C, D.
Класи за ISO 14644-1
Чим нижчий номер класу — тим чистіше приміщення. Наприклад:
-
ISO 5 використовується у фармацевтичних зонах з підвищеним рівнем стерильності.
-
ISO 8–9 — менш строгі зони, наприклад, підготовчі технічні приміщення.
Класи за GMP
Це більш прикладні (практичні) категорії, що застосовуються для зон стерильного та нестерильного виробництва:
-
Клас A — найбільш критичні процеси (розлив, асептичне наповнення).
-
Клас B — фонове середовище для класу A.
-
Класи C і D — зони підтримки та підготовчі кімнати.
Таким чином, система класів дозволяє точно визначити, наскільки жорсткі умови потрібні для конкретного технологічного етапу.
Стандарти GMP для чистих приміщень
GMP-стандарти — це комплекс правил належної виробничої практики, обов’язкових для фармацевтичної, біотехнологічної та медичної промисловості.
Вимоги GMP для чистих приміщень охоплюють:
-
конструкцію і матеріали (гладкі, безшовні, вологостійкі, антистатичні поверхні);
-
системи вентиляції й фільтрації (HEPA/ULPA);
-
перепад тиску між зонами;
-
класифікацію та моніторинг повітря;
-
правила поведінки персоналу і гігієну;
-
контроль технологічних процесів та документацію.
Виконання стандартів GMP для чистих приміщень є необхідною умовою для отримання дозволів, сертифікації виробництва та виходу продукції на світові ринки.
ISO-сертифікація чистих приміщень в Україні
Вимоги ISO 14644 застосовуються у багатьох галузях, що потребують точності та відсутності мікрочастинок:
ISO чисті приміщення Україна — один із найзатребуваніших запитів від підприємств, що проходять аудит або готуються до сертифікації. Стандарт ISO 14644 визначає вимоги до:
-
вимірювання концентрації частинок у повітрі;
-
типів фільтрів та вентиляційних систем;
-
конструктивних матеріалів;
-
систем герметизації стиків;
-
планування зонованості (чисті/забруднені коридори).
Для отримання сертифікації важливо мати відповідну документацію, результати тестів, протоколи вимірювань та підтверджену відповідність конструктивних рішень.
Чому чисті приміщення є критично важливими для виробництва
Використання чистих приміщень забезпечує:
-
мікробіологічну безпеку продукції;
-
передбачуваність і стабільність технологічних процесів;
-
допуск до міжнародних ринків завдяки відповідності GMP та ISO;
-
зменшення виробничих ризиків;
-
підвищення строку придатності та якості продукції;
-
покращення репутації виробника та довіри партнерів.
Для фармацевтичної та біотехнологічної сфер наявність таких приміщень — не конкурентна перевага, а обов’язкова вимога.
Чисте приміщення — це високотехнологічний простір із контрольованим середовищем, створений для забезпечення бездоганної якості виробництва. Вимоги GMP і ISO регламентують усе: від вибору матеріалів до режиму роботи вентиляційних систем. Підприємства, які дотримуються цих стандартів, отримують доступ до міжнародних ринків та гарантують безпеку своєї продукції.